본 컨텐츠는 AI를 이용한 컨텐츠로, AI기술이 가진 구조적 한계를 가지고 있습니다.
- 바이오 제약 회사인 슈퍼누스 파머슈티컬스는 파킨슨병에 대한 임상시험용 아포모르핀 주입 장치인 SPN-830에 대한 규제 업데이트를 발표했습니다.
- 미국 FDA는 현재 신청서 양식으로는 승인할 준비가 되지 않았다는 내용의 완전 답변서를 발행했습니다.
- NDA를 다시 제출하려면 주입 장치에 대한 추가 제품 품질 데이터와 정보가 필요합니다.
- 임상 안전성 또는 유효성 문제는 확인되지 않았으며, 장치 제조업체의 시설에 대한 사전 승인 검사가 성공적으로 완료되었습니다.
- 슈퍼누스 파머슈티컬스는 FDA와 협력하여 CRL을 해결하고 PD 환자를 위한 치료 옵션으로서 SPN-830을 성공적으로 시장에 출시하기 위해 최선을 다하고 있습니다.
[보도자료 원본 보기]
[기업개요]
슈퍼너스 파마슈티컬스는 중추신경계 질환 치료를 위한 제품 개발 및 상용화에 주력하는 제약 회사입니다. 회사는 뇌전증 환자를 위한 두 가지 치료제인 옥스텔라 XR(서방형 옥스카바제핀)과 트로켄디 XR(서방형 토피라메이트)을 제공합니다.
또한 충동적 공격성(IA) 치료와 주의력 결핍 과잉행동 장애(ADHD) 치료의 미충족 의료 수요와 시장 기회를 해결하기 위해 정신과 분야에서 여러 제품 후보를 개발 중입니다.
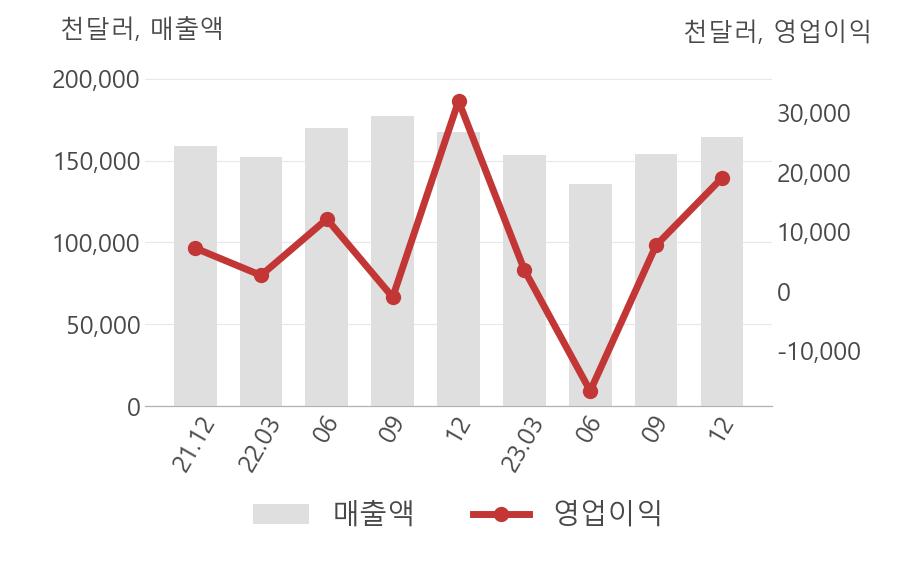
[최근실적추이]