본 컨텐츠는 AI를 이용한 컨텐츠로, AI기술이 가진 구조적 한계를 가지고 있습니다.
FDA 자문위원회는 3등급 노출성 다발성 골수종에 대해 Abecma에 찬성표를 던졌습니다.
- Abecma에 대한 추가 생물학적 제제 허가 신청은 아직 FDA 검토 중입니다.
- Abecma는 일본과 스위스에서 승인을 받았으며 CHMP로부터 긍정적인 의견을 받았습니다.
- FDA는 sBLA 검토를 위한 새로운 목표 조치 날짜를 정하지 않았습니다.
- 브리스톨 마이어스 스퀴브와 2세븐티 바이오는 도움이 필요한 더 많은 환자들에게 Abecma를 제공할 수 있을 것으로 낙관하고 있습니다.
[보도자료 원본 보기]
[기업개요]
2세븐 바이오는 세포 및 유전자 치료 회사로, 암에 대한 혁신적 치료법의 연구, 개발 및 상용화에 주력하고 있습니다. 투세븐 바이오는 T 세포 공학 기술과 렌티바이러스 벡터 유전자 전달 접근법에 대한 전문 지식, 세포 치료제의 연구, 개발 및 제조 경험, 암 환자를 위한 표적 세포 치료제를 개발하기 위해 선택적으로 배치할 수 있는 일련의 기술을 결합하여 접근합니다.
회사는 재발성 및 난치성 급성 골수성 백혈병(AML) 소아 환자 치료를 위한 SC-DARIC33, B세포 비호지킨 림프종(B-NHL) 환자 치료를 위한 bbT369 등 다수의 임상 프로그램과 MUC16을 표적으로 하는 조작된 CAR T 세포 치료제인 bbT4015 등 다수의 전임상 프로그램을 진행하고 있다.
또한 파트너사인 브리스톨 마이어스 스퀴브와 함께 미국 내 다발성 골수종 환자들에게 아벡마를 공급하고 있습니다.
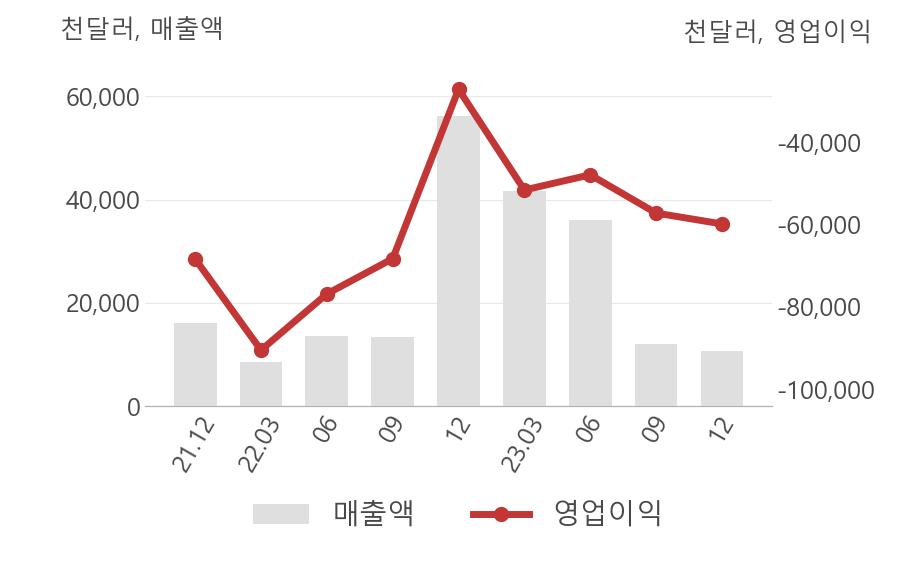
[최근실적추이]